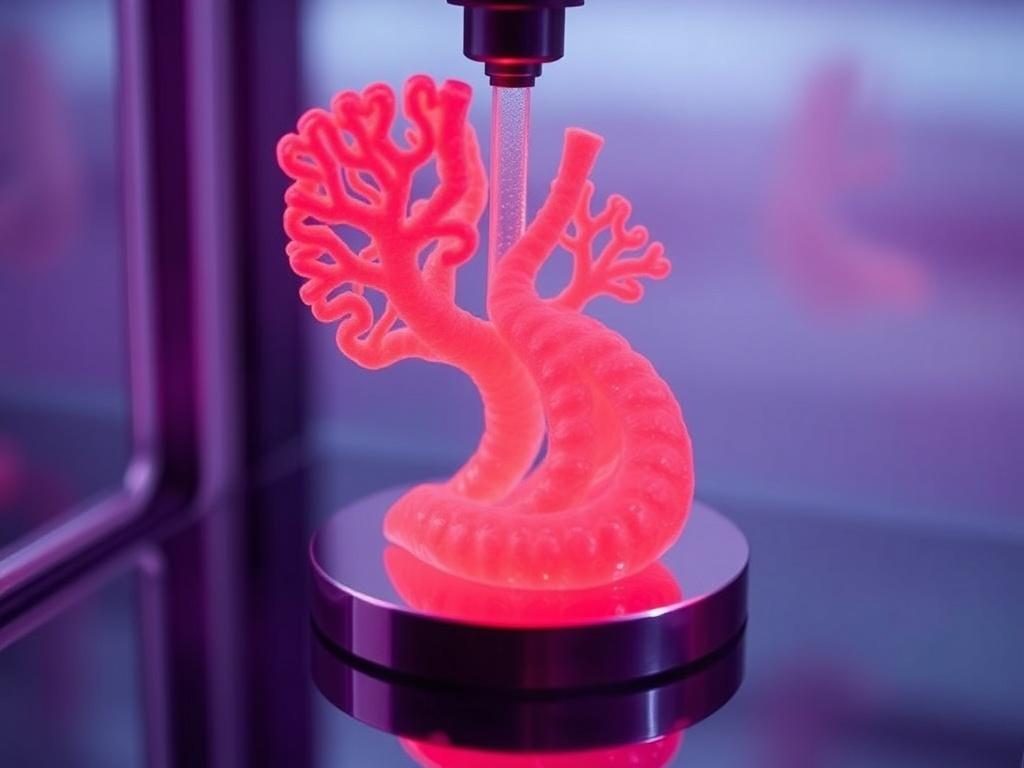
Вообразите устройство, которое может укладывать на поверхность микро-слой за слоем живые клетки, формируя зачатки тканей и даже целые органы. Биопринтеры обещают перевести мечты биоинженеров из лабораторий в реальность клиник. Однако за сияющей картиной стоят сложные механизмы, био-материалы и принципы биологической совместимости. В этой статье мы разберем, как работают биопринтеры, чем они могут обогатить медицину сегодня и какие вызовы стоят перед исследователями на пути к печати полноценной ткани или органа.
Как задумано и зачем вообще нужна биопечать
Идея печати живых тканей пришла к ученым после того, как стало понятно, что традиционные методы культивирования клеток в чашках Петри далеко не всегда дают нужную структуру для функционирования в организме. Ткани и органы представляют собой не просто набор клеток, но сложную архитектуру, где клетки взаимодействуют друг с другом, образуют сосудистую сеть и реагируют на механические сигналы. Биопринтеры призваны воспроизвести эту архитектуру с контролируемой точностью. Это открывает путь к созданию моделей заболеваний, тестированию лекарств без животных и, в перспективах, к резидентной замене фрагментов тканей больного человека.
Ключевое преимущество биопечати — способность работать с индивидуальными параметрами пациента. Можно настроить параметры биоматериалов и клеточные композиции под конкретного пациента, чтобы минимизировать риск иммунного отторжения после трансплантации. В условиях современной медицины такие технологии могут уменьшить время ожидания донорских органов, сократить расходы на реабилитацию и повысить точность диагностики за счет прецизионной реплики тканей. Но это путь, где на первом плане стоят не одно лишь технологические хитрости. Здесь важна биологическая реалистичность, безопасность и регуляторная прозрачность.
Как устроены современные биопринтеры
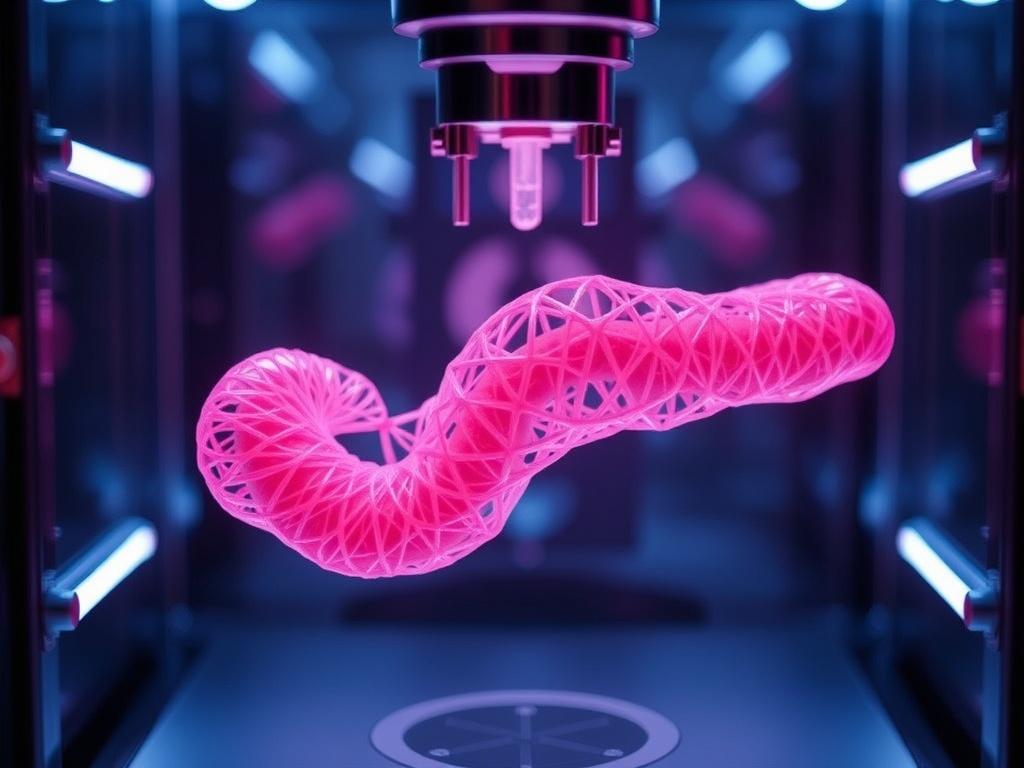
Биопринтер — это не просто принтер. Это система, которая объединяет три ключевых элемента: подачу клеточных суспензий или биоматериалов, точную координацию по координатам и контроль условий окружающей среды во время печати. В основе лежит понятие «биоматериал» — гумификация, которая обеспечивает клеткам нужную опору и защиту, а иногда и сигнальные молекулы для их функций.
Существуют различные принципы подачи материала. В одних системах материал выдавливается через экструдер, в других — распыляется или во времени подается каплями. В лазерно-ассистированной печати применяется энергия лазера для локального переноса биоматериала. Каждый метод имеет свои преимущества и ограничения: точность, скорость, восприимчивость клеток, сложности с сосудистыми сетями и стоимость оборудования. В совокупности эти подходы создают палитру инструментов для решения самых разных задач — от печати кожных покровов до структур внутри органов.
Говоря простыми словами, биопринтеры работают как конструктор из мельчайших деталей, но вместо обычных материалов там применяются живые клетки и биоматериалы. Важный момент: клетки не только размещаются на нужной поверхности, но и должны сохранять жизнеспособность и способность к функционированию в будущей ткани. Поэтому выбор среды для печати, типа клеток и режимов печати подбирается таким образом, чтобы минимизировать стресс и обеспечить нормальные клеточные взаимодействия.
Ключевые материалы и клеточные компоненты
В биопечати применяют три основных элемента: клетки, биоматериалы-носители и факторы роста. У клеток есть свои требования к питательной среде, температуре и уровню питательных веществ. Биоматериалы хорошо удерживают форму и могут поддерживать клеточные контакты, помогая тканям развиваться. Факторы роста управляют поведением клеток — делением, миграцией и специализацией. Вместе эти компоненты формируют «биопечальную пасту», которая во время печати сохраняет жизнеспособность и функциональность.
Клеточный материал чаще всего готовят из стволовых клеток, которые способны превратиться в нужный тип ткани. Это могут быть индуцированные плюрипотентные стволовые клетки (iPSCs), клетки кожи, мышцы, сосудистый эндотелий и прочие. В некоторых случаях используют трансплантированные клетки донора, а в других — клетки самого пациента. Вопрос совместимости и риск иммунного ответа остаются центральной задачей в теме биопечати.
Биоматериалы-носители (гидрогели, полимеры и композиты) должны быть biocompatible и в то же время обеспечивать нужную механическую прочность. Гидрогели часто напоминают мягкую матрицу ткани, и они позволяют клеткам расти, образуя межклеточные контакты. Но не все гидрогели одинаково хороши для каждого типа ткани. Поэтому исследователи подбирают состав и концентрацию так, чтобы сохранить структуру печатной заготовки и обеспечить последующее развитие ткани в живом организме.
Методы биопечати: как именно формируют слои
Существуют три базовых метода, на которых строится современная биопечать. Каждый из них подходит под разные задачи и имеет свои сильные стороны. В повседневной практике исследователи часто комбинируют методы, чтобы добиться необходимой плотности ткани, точности размещения клеток и функциональности.
Экструзионная биопечать
Этот метод напоминает обычную экструзию пасты через мелкую трубку. Жидкость с клетками и гидрогелью выдавливается в виде линий, образуя слои. Экструзионная печать хорошо подходит для построения высокообъёмных структур и для воплощения сложных каркасных форм. Она обеспечивает большую скорость по сравнению с другими подходами и позволяет использовать разнообразные биоматериалы.
Однако здесь существуют ограничения. Давление и вязкость материалов должны быть подобраны так, чтобы сохранить жизнеспособность клеток. Слишком сильное давление может повредить клетки, а слишком плотная паста — ограничить их движение и рост. Исследователи работают над оптимизацией параметров: скорости подачи, диаметра иглы, температуры и состава суспензии. В итоге получаются трёхмерные заготовки, которые затем проходят этапе адаптации и культивирования в биореакторе.
Инкжекционная базовая печать (inkjet)
Метод капельной печати развивает идею принтерной печати мелких капель — каждая капля содержит часть клеток и матрицу. Капли располагаются точечно на подложке, создавая по слоям желаемую тканевую карту. Этот подход даёт высокую точность размещения и минимальное разрушение клеток, поскольку давление и деформация минимальны.
Проблема в том, что капли должны быть достаточно стабильны во время печати, чтобы сохранить форму. Иногда капли капсулируются в гидрогели или гелеобразные носители, чтобы повысить устойчивость и обеспечить дальнейшее развитие ткани. Также важна скорость печати и полнота заполнения пор. Капельная биопечать особенно эффективна при создании тонких слоёв, микро архитектур и тканевых моделей поверхностных структур, таких как кожа или слизистые оболочки.
Лазерно-ассистированная биопечать
Этот метод использует лазер для переноса клеток с подложки на поверхность печати. Лазерная энергия позволяет очень точно перемещать клеточную массу без механического воздействия, что снижает риск повреждений. Такой подход обеспечивает исключительную точность и способность работать с чувствительными клетками.
Недостаток лазерной печати — технологическая сложность и стоимость оборудования. Также требуется строгий контроль параметров лазера, чтобы не повредить клетки и сохранить их функциональность. В совокупности лазерная биопечать находит применение там, где нужна высокая точность распределения клеток и минимальное вмешательство в их жизнеспособность. В сочетании с подходами экструзии или капельной печати он образует мощный арсенал инструментов для создания сложных тканевых структур.
Применение биопечати в медицине и научных исследованиях
Сферы применения биопечати уже сейчас охватывают модели заболеваний, тесты лекарств, персонализированную медицину и, по мере прогресса, потенциальную клиническую трансплантацию. Ниже — ключевые направления и реальные примеры.
Первая волна применения — создание тканевых моделей для изучения заболеваний и тестирования лекарств. К примеру, печать тканевых пластов из печени или почек позволяет исследовать, как препараты влияют на клеточные функции в условиях, близких к естественным. Такие модели сокращают зависимость от животных тестов и дают более точные данные о реакции человеческих органов на препараты.
Вторая волна — кожные имплантаты и регенеративная медицина. Печать кожи может помочь ускорить заживление ран, создать сложные кожные пласты для ожогов или травм. В них часто включают линии кровоснабжения и нервных элементов, чтобы рана зажила не только закрытием поверхности, но и возвращением функциональности. Это направление особенно активно развивается в клиниках хирургов и дерматологов.
Третья волна — печать сосудистых сетей и органов. Без развитой сосудистой системы ткани не может выжить в больших объемах. Исследователи работают над созданием миниатюрной сети кровеносных сосудов внутри печатных конструкций. Это критический шаг на пути к созданию более крупных пластов ткани и даже к печати отдельных органов в будущем. В рамках учебно-биологической печати сосудистая сеть становится ключевым элементом для гипсовых моделей в лаборатории, а затем и для биологической жизни внутри человека.
Таблица: сравнение основных методов биопечати
| Метод | Принцип | Преимущества | Ограничения |
|---|---|---|---|
| Экструзионная биопечать | Выдавливание суспензии через иглу или сопло | Высокая скорость, подходит для крупных структур, поддерживает разнообразные биоматериалы | Риск травмы клеток от давления, ограничения по вязкости материалов |
| Инкжекционная (капельная) печать | Подача капель с клетками по точкам на подложке | Высокая точность размещения, низкая механическая нагрузка на клетки | Искусственные ограничения по стабильности капель, сложная консолидация слоев |
| Лазерно-ассистированная печать | Лазер переносит клетку на поверхность печати | Максимальная точность, минимальное механическое воздействие | Высокая стоимость, техническая сложность |
Клиника и регуляторика: путь к применению в медицинской практике
Новизна биопечати сталкивается с требованиями регуляторных органов и безопасности пациентов. Любая клиническая реализация должна пройти серию испытаний на биосовместимость, жизнеспособность клеток, потенциал к опухолевому росту и долгосрочную стабильность тканей. Прямые трансплантации полностью распечатанных органов пока далеки от повседневной клиники, но появляется всё больше работ по печати гетеротопических структур или композитов, которые могут служить временными заменителями или моделями для предоперационных планов.
Этические вопросы остаются важной темой обсуждений. В центре — источники клеток и использование стволовых клеток. Вопросы безопасности, приватности данных пациентов и доступности новых технологий для широкого круга населения требуют прозрачности и ответственного подхода. Но регуляторные органы разворачивают дорожные карты, которые помогают переводить исследования в клинику без потери надзора за безопасность и этику.
Как устроены лабораторные процессы: от идеи к готовой заготовке
Рабочий процесс в лаборатории биопечати начинается с разработки архитектуры ткани. Исследователь выбирает тип ткани и параметры: клетки, носитель, факторы роста, условия культивирования. Затем создают модель 3D-структуры в компьютерной программе, которая генерирует слоистую карту для принтера. В процессе печати контролируется каждое перемещение насадки относительно координатной сетки. После печати заготовку удерживают в биореакторе, где подводят питательные растворы, регулируют температуру и влажность, чтобы клетки могли развиваться и становится функциональной тканью.
Особое внимание уделяется биодоступности и стимуляции клеток. В некоторых случаях в заготовку добавляют сигнальные молекулы, которые помогают клеткам дифференцироваться в нужные типы тканей. Например, для печени применяются комбинации факторов роста, которые приводят клетки к функциональной функции подобных печёночной ткани. В других случаях требуется построение капиллярной сети, чтобы обеспечить клетки кислородом и питательными веществами. Это один из самых сложных аспектов биопечати сегодня.
Системы контроля качества играют ключевую роль. По мере продвижения проекта исследователи проводят анализ жизнеспособности клеток, активность генов и функциональные тесты. В некоторых проектах применяют не только клетки, но и сенсоры для контроля pH, температуры и других параметров в реальном времени. Такой комплекс обеспечивает уверенность, что печатные конструкции смогут выживать и функционировать после переноса в живой организм.
Элементы успеха: клеточные платформы и регуляторы
Еще одна важная нить в теме биопечати — выбор клеточных платформ. Итоговая ткань зависит от того, какие клетки и в каком сочетании применяются. На практике чаще всего работают с клетками человека, чтобы повысить шансы на биологическую совместимость. Важен не только тип клеток, но и их состояние на момент печати: клетки в состоянии активного деления могут выжить, но быстро теряют функциональность, если условия не поддерживают их дифференциацию и специализацию.
Говоря о регуляторах, стоит упомянуть роль биомаркеров, которые позволяют отслеживать процесс дифференциации клеток и формирование специфических функций ткани. В некоторых проектах применяют биосенсоры, чтобы фиксировать присутствие критически важных факторов роста и их локализацию внутри печатной заготовки. Это помогает исследователям корректировать параметры на лету и добиваться более надёжных результатов.
Персонализация и будущее трансплантации

Одна из самых волнующих тем — персонализированная биопечать. Представьте, что можно взять клетки пациента, создать из них нужный тип ткани и напечатать тканевую замену, идеально адаптированную к анатомии конкретного человека. Это снизит риск иммунного отторжения и может ускорить заживление после операции. В реальности на ранних стадиях такие проекты чаще рассматриваются с целью создания моделей и предоперационного планирования. Но тенденции указывают на рост клинического применения в ближайшие годы.
С точки зрения будущего, биопринтеры скорее станут частью полного цикла регенеративной медицины. Мы можем видеть сценарии, где печатные заготовки интегрируются с собственными клеточными платформами пациента, где после трансплантации ткань продолжает развиваться под контролем тела. В этом сценарии биоматериалы и клетки взаимодействуют как единая система, что позволяет organ-on-a-chip моделям перейти к полноценной органной функциональности. Это потребует не только технологической эволюции, но и совершенствования клинических протоколов и регуляторной базы.
Личный опыт автора и примеры из жизни науки
Я часто думаю о биопринтинге как об удивительном синтезе инженерной точности и биологической живости. Когда в университетской библиотеке мы смотрели на первые публикации по лазерной биопечати, казалось, что это фантазия. Но спустя годы видно, как эти идеи превратились в реальные прототипы — от печати кожных пластов для ожоговых ран до создания моделей печени для тестирования лекарств. В рамках одного проекта мы столкнулись с вызовом: как сохранить жизнеспособность клеток в зоне распыления и при этом сохранить нужную архитектуру. Эксперимент был рискованным, но в итоге мы увидели, как клетки начали формировать первые признаки дифференцировки. Такой опыт напоминает не только лабораторную работу, но и творческий процесс художника, который выстраивает композицию из деталей, чтобы получить органическую целостность.
Из реальных примеров можно привести опыт в США и ЕС, где исследователи создают печатные модели кожи, печатные модели сосудов и даже небольшие заготовки печени для тестирования лекарств. В одном известном проекте ученые работали над созданием реальных кожных покровов с нервной сетью — зачатковыми элементами, которые позже должны стать полноценной функциональной кожей. Этот пример показывает, как биопринтеры уходят от лаборатории к клинике и начинают встраиваться в реальные медицинские задачи.
Этические и социальные аспекты
С ростом возможностей биопечати возрастает внимание к этике и социальным эффектам новых технологий. Вопросы доступа к лечению и равенства в здравоохранении становятся не менее важными, чем технологические достижения. Кто будет иметь доступ к печати тканей и органов на высоком уровне? Какие стандарты качества должны быть введены для снижения рисков? Ответы на эти вопросы требуют совместной работы регуляторов, ученых, клиницистов и общества.
Немаловажна и безопасность данных пациентов, чьи клетки используются для печати. Нужно обеспечить защиту биоматериалов и персональных данных, чтобы исключить злоупотребления и коммерциализацию без согласия. В условиях быстро развивающейся отрасли каждая страна формирует свои протоколы и дорожные карты. Это естественный процесс, который в итоге укрепит доверие к биопечати и ускорит ее внедрение в клиническую практику.
Как двигаться дальше: советы для тех, кто хочет быть в авангарде биопечати
Если вам интересна биопечать, начните с основоположных знаний в биологии клетки, материаловедении и инженерии. Освойте принципы трех базовых методов печати, поймите различия между гидрогелями и полимерами, научитесь анализировать клеточные культуры и работать с биореакторами. Важно также освоить компьютерное моделирование для создания трёхмерных архитектур тканей. Эти навыки будут полезны как исследователю, так и инженеру, работающему над прототипами биопечати.
Практический путь включает участие в проектах по созданию тканевых моделей, участие в лабораториях с доступом к биопечати и знакомство с клиницистами, которые могут объяснить реальные медицинские потребности. Нельзя забывать о нормативной базе и этике, потому что эти моменты напрямую влияют на скорость переноса из лаборатории в клинику. Постепенно вы будете накапливать опыт и сможете вносить вклад в развитие новых подходов — от печати кожи до построения сосудистых сетей внутри печатных заготовок.
Перспективы и вызовы, которые формируют будущее
Развитие биопечати требует комплексного подхода. В ближайшие годы мы увидим усиление междисциплинарной кооперации между биологами, инженерами, химиками и клиницистами. Это сотрудничество поможет ускорить создание функциональных тканей и минимизировать риски при клиническом применении. Важной задачей остается развитие сосудистых сетей внутри печатных конструкций, чтобы обеспечить жизнеспособность больших тканей и органов.
Непредсказуемость биологической системы требует гибких и адаптивных стратегий. Мы будем видеть переход от экспериментальных прототипов к более устойчивым решениям, которые можно будет масштабировать. В какой-то момент биопринтеры станут неотъемлемой частью хирургических операций, когда печатные пласты будут интегрированы в живой организм и помогать восстанавливать утраченные функции после травм или болезней. Однако на этой дороге впереди множество шагов, требующих времени, инвестиций и строгого контроля качества.
Инструменты и таблицы полезных сведений
В практическом руководстве по биопечати полезно держать под рукой несколько инструментов и критериев. Ниже — компактный набор ориентиров, который может помочь студентам и начинающим исследователям ориентироваться в теме.
- Выбор метода печати зависит от требуемой структуры ткани, размеров заготовки и чувствительности клеток.
- Гидрогели-носители должны сочетать механическую прочность и биосовместимость, а также поддерживать нужные сигнальные молекулы.
- Клеточные композиции подбираются с учётом возможности дифференциации и функциональности ткани.
- Критически важно обеспечить питание клеток и создаваемой ткани в процессе культивирования.
Далее можно рассмотреть две практические схемы для обсуждения в классе или на семинаре. В схеме A — печать кожи с включением сосудов, где нужно обеспечить сетку кровоснабжения. В схеме B — печать миниатюрной печени для моделирования лекарственной реакции. Эти сценарии помогают перейти от абстрактных концепций к конкретным задачам и формируют представление о том, какие шаги нужно предпринять на разных стадиях проекта.
Заключение без слова «заключение»: итог размышлений
Биопринтеры держат оборону на пересечении инженерии и биологии. Они не просто копируют естественную ткань, они создают архитектуру, в которой живые клетки получают необходимую опору и сигналы для функционирования. Техническая грамотность, продуманная биоматериализация и этическая ответственность — три столпа, на которых стоит развитие этой области. Уже сегодня биопечать приносит ощутимую пользу для исследований и моделирования заболеваний, а в обозримом будущем она может радикально изменить подход к лечению травм и дегенеративных болезней.
Каждый новый прототип — шаг к более масштабной клинике. Каждый успех — напоминание о том, что на стыке науки и медицины рождается не просто частный случай, а новая парадигма, которая может изменить отношение общества к здоровью. Биопринтеры продолжают учиться на ошибках, на опыте предыдущих проектов и на пожеланиях клиницистов. И если сейчас мы видим только зачатки сложной ткани, то завтра эти зачатки могут стать полноценной жизнью, возвращая людям здоровье и качество жизни. В этом пути важно помнить: впереди путь долгий, но каждый шаг приближает нас к цели — понять и воспроизвести живое творение природы с точностью инженерной карты и ответственностью медицинестской практики.