Фенолы – органические соединения. Они в небольших количествах есть в природе. Основную массу фенола и производных на его основе получают синтетическим путём.
По числу гидроксильных групп:
- фенолы с одной группой ОН — содержат одну группу -ОН. Общая формула CnH2n-7OH или CnH2n-6O.
- фенолы с двумя группами ОН — содержат две группы ОН. Общая формула CnH2n-8(OH)2 или CnH2n-6O2.

| Соединения, в которых группа ОН отделена от бензольного кольца углеродными атомами – это не фенолы, а ароматические спирты: |

В фенолах одна из неподеленных электронных пар кислорода участвует в сопряжении с π–системой бензольного кольца, это является главной причиной отличия свойств фенола от спиртов.

| Сходство и отличие фенола и спиртов.
Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода. Отличия:
|
1. Кислотные свойства фенолов
| Фенолы являются более сильными кислотами, чем спирты и вода, т. к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается. |
Раствор фенола в воде называют «карболовой кислотой», он является слабым электролитом.
1.1. Взаимодействие с раствором щелочей
В отличие от спиртов, фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты.
| Например, фенол реагирует с гидроксидом натрия с образованием фенолята натрия |

Видеоопыт взаимодействия фенола с гидроксидом натрия можно посмотреть здесь.
Так как фенол – более слабая кислота, чем соляная и даже угольная, его можно получить из фенолята, вытесняя соляной или угольной кислотой:

1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Фенолы взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются феноляты. При взаимодействии с металлами фенолы ведут себя, как кислоты.
| Например, фенол взаимодействует с натрием с образованием фенолята натрия и водорода. |

Видеоопыт взаимодействия фенола с натрием можно посмотреть здесь.
Источник: http://chemege.ru/fenoly/
Что такое фенол
К фенолам относят производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с фенил радикалом. Они могут иметь одну или несколько гидроксогрупп.
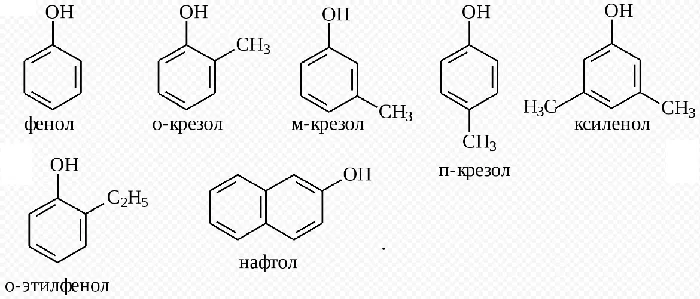
Самым простым представителем этой группы соединений считают фенол. Он и дал название классу веществ. Это же соединение называют гидроксибензолом.
Источник: http://nauka.club/khimiya/fenoly.html
Поликонденсация в кислой среде
При кислотном катализе реакция протекает по следующему механизму. Сначала происходит протонизация формальдегида:
Далее возникший карбониевый ион атакует фенол, образуя ион гидроксиметилфенола:В кислой среде гидроксиметилфенолы образуют сравнительно устойчивые и долгоживущие карбониевые ионы, которые реагируют как электрофильные агенты с фенолом или его гидроксиметильными производными:В общем виде процесс получения новолака может быть представлен схемой:Уменьшение избытка фенола в исходной смеси сопровождается возрастанием молекулярной массы образующегося новолака, и при соотношении, близком к эквимольному, можно получить полимер пространственного строения.
В молекулах новолаков, полученных из трифункционального фенола или смеси фенолов, содержащей хотя бы один трифункциональный фенол, еще остаются активные атомы водорода в орто- и пара – положениях к фенольным гидроксилам. Поэтому при обработке их формальдегидом заменив кислотный катализатор основным, можно получить резол непосредственно неплавкий и нерастворимый полимер резит.
Резит получается также при действии на новолак полимеров формальдегида (параформ, α-полиоксиметилен, β-полиоксиметилен) или гексаметилентетрамина. В последнем случае, по-видимому, в процессе отверждения участвуют ди- и триметиламины, образующиеся при разложении гексаметилентетрамина, а выделяющийся аммиак играет роль катализатора.
Новолаки, полученные из бифункциональных фенолов (о- и п-крезолов), при обработке формальдегидом не переходят в неплавкое и нерастворимое состояние. Однако если такие олигомеры нагревать выше 180 °С, они способны переходить, хотя и медленно, в неплавкое и нерастворимое состояние.
Аналогичная картина наблюдается при 250—280 °С и для новолаков, получаемых поликонденсацией 1 моль фенола с 0,8 моль формальдегида, что можно объяснить активацией атомов водорода в мета-положении к фенольным гидроксилам или взаимодействием последних с образованием эфирных связей.
Источник: http://mplast.by/encyklopedia/sintez-fenoloaldegidnyih-polimerov-osobennosti-protsessov-polikondensatsii/
Физические свойства фенола
Фенол-твердое, бесцветное кристаллическое вещества, t°плавления=43°С, t°кипения=181°С, с резким характерным запахом.Ядовит.Фенол при комнатной температуре незначительно растворяется в воде. Водный раствор фенола называют карболовой кислотой.При попадании на кожу он вызывает ожоги,поэтому с фенолом нужно обращаться очень осторожно!
Источник: http://himege.ru/fenoly-nomenklatura-poluchenie-ximicheskie-svojstva/
Общая и структурная формулы
Состав веществ можно выразить общей формулой С6Н6-n(ОН)n.
Простейший представитель класса имеет 1 гидроксогруппу. Его молекулярная формула С6Н5ОН. Структурная формула — ОН.
Если в молекуле фенола 1 атом водорода заместить на метильный радикал, получим метилфенол. Если к нему прибавить ещё одно бензольное ядро, получим нафтол.
Источник: http://nauka.club/khimiya/fenoly.html
Свойства
- механическая устойчивость, прочность
- коррозионная устойчивость
- высокие электроизоляционные свойства
- отличная растворимость в алифатических и ароматических углеводородах, хлорсодержащих растворителях и кетонах. Растворимы в водных растворах щелочей и полярных растворителях, после отверждения превращаются в густосшитые полимеры аморфной микрогетерогенной структуры.
Источник: http://wiki2.org/ru/Фенолформальдегидная_смола
Применение материала
Фенолформальдегидная смола применяется в разных сферах деятельности, с помощью нее в промышленности изготавливают разные классы пластмассы. Использование в быту популярно, разный пластик получают при разном типе воздействия. Пластмасса часто используется в медицине.
Фенолформальдегид применяется при производстве лаковой продукции, клеевых растворов, герметиков.
Так она применяется для производства следующих изделий:
- Тормозные колодки в поездах, элементы автомобиля и т.п.;
- Абразивные приспособления;
- Детали электрических приборов;
- Корпусные части смартфонов;
- В радио-промышленной сфере;
- Для изготовления оружия и другой военной техники;
- Для изготовления посуды, которую не подвергают нагреву;
- Для бижутерии, сувенирной продукции;
- Другое.
Не используется смола для изделий, которые будут напрямую контактировать с пищей.

Фенолформальдегидная смола применяется в разных сферах деятельности, с помощью нее в промышленности изготавливают разные классы пластмассы.
Источник: http://kraski-net.ru/spetsialnye-materialy/dopolnitelnye-sredstva/svojstva-primenenie-i-strukturnaya-formula-fenolformaldegidnoj-smoly
3. Поликонденсация фенола с формальдегидом
С формальдегидом фенол образует фенолоформальдегидные смолы.

Источник: http://chemege.ru/fenoly/
4. Взаимодействие с хлоридом железа (III)
При взаимодействии фенола с хлоридом железа (III) образуются комплексные соединения железа, которые окрашивают раствор в сине-фиолетовый цвет. Это качественная реакция на фенол.
Видеоопыт взаимодействия фенола с хлоридом железа (III) можно посмотреть здесь.
Источник: http://chemege.ru/fenoly/
Экологические аспекты
В производстве применяются токсичные материалы. И фенол, и формальдегид ядовиты и огнеопасны.[3] Формальдегид обладает канцерогенным, а также угнетающим воздействием на нервную систему.
Фенолформальдегидные смолы могут оказывать вредное воздействие на кожу, они могут вызывать дерматиты и экземы.[3] Неотверждённая фенолформальдегидная смола может содержать до 11 % свободного фенола.[4]
При отвержении фенолформальдегидных смол в пластмассе (фенопласты) происходит сшивка олигомерных фрагментов смолы с участием содержащегося в ней свободного фенола, при этом содержание фенола, инкорпорированного в фенопласте, снижается до следовых количеств; санитарными нормативами РФ регламентируются допустимые количества миграции фенола и формальдегида для изделий из фенопластов; в частности, для изделий, контактирующих с пищевыми продуктами для фенола — 0,05 мг/л, для формальдегида — 0,1 мг/л[5].
Большой проблемой является сложность утилизации или повторного использования изделий из фенолформальдегида.
Источник: http://wiki2.org/ru/Фенолформальдегидная_смола
Экологические аспекты
Для экологии использование ядовитых компонентов при производстве смолы становится опасностью. Проблемой считается вредность токсичных элементов, а именно процесс их утилизации. Так СанПиН следит за использование элементов, и количеством которые применяются.

Для экологии использование ядовитых компонентов при производстве смолы становится опасностью.
Источник: http://kraski-net.ru/spetsialnye-materialy/dopolnitelnye-sredstva/svojstva-primenenie-i-strukturnaya-formula-fenolformaldegidnoj-smoly
Примечания
 Эта страница в последний раз была отредактирована 2 марта 2021 в 13:54.
Эта страница в последний раз была отредактирована 2 марта 2021 в 13:54. Как только страница обновилась в Википедии она обновляется в Вики 2.
Обычно почти сразу, изредка в течении часа.
Источник: http://wiki2.org/ru/Фенолформальдегидная_смола
2. Кумольный способ
Фенол в промышленности получают из каталитическим окислением кумола.
Первый этап процесса – получение кумола алкилированием бензола пропеном в присутствии фосфорной кислоты:

Второй этап – окисление кумола кислородом. Процесс протекает через образование гидропероксида изопропилбензола:

Суммарное уравнение реакции:

Источник: http://chemege.ru/fenoly/
Биоразложение
Фенолформальдегид разлагается грибком белой гнили Phanerochaete chrysosporium .
Источник: http://ru.other.wiki/wiki/Phenol_formaldehyde_resin
3. Замещение сульфогруппы в бензол-сульфокислоте
Бензол-сульфокислота реагирует с гидроксидом натрия с образованием фенолята натрия:

Получается фенолят натрия, из которого затем выделяют фенол:
Источник: http://chemege.ru/fenoly/
Смотрите также
- Карбамидоформальдегид
- Паратретичная бутилфенолформальдегидная смола
Источник: http://ru.other.wiki/wiki/Phenol_formaldehyde_resin
Этерифицированные смолы
Этерификация способствует соединению смолы с растительными маслами и иными типами смол. Процесс производится с помощью бутилового спирта. Так при определённых условиях можно, например, получить бутоксикрезолоформальдегидную смолу РБ.
Смола производится растворного типа в бутаноле, выделится нижеописанными свойствами:
- Бесцветная жидкость с желто-красным оттенком по виду;
- Уровень вязкости ВЗ4 при 2-градусном воздействие составляет 100-300с.
Данный тип материала используется в 60%-растворе для изготовления электроизоляционных лаковых продуктов (Фл-98, ПЭ-933).

Процесс производится с помощью бутилового спирта.
Фенолформальдегидная смола позволяет повысить качество разнообразной продукции, с помощью нее производят различные материалы. Она отличается рядом положительных свойств. Но является опасным веществом, поэтому при производстве должны соблюдаться правила СанПиНа. Ее изобретение важным звеном для получения разнообразных материалов.
Источник: http://kraski-net.ru/spetsialnye-materialy/dopolnitelnye-sredstva/svojstva-primenenie-i-strukturnaya-formula-fenolformaldegidnoj-smoly
